Sección: Avances de Investigación
DRA. MARÍA AMPARO RODRÍGUEZ-SANTIAGO
ORCID 0000-0003-0616-237X
PAS. BIOL. CELSO RUBÉN CANCHE-TUN
ORCID 0000-0001-5118-5058
DR. ENRIQUE ÁVILA
ORCID 0000-0001-7074-1603
DR. JOSÉ IANNACONE
ORCID 0000-0003-3699-4732
DR. GEORGE ARGOTA-PÉREZ
ORCID 0000-0003-2560-6749
Recibido: 16 de mayo de 2024.
Aceptado: 27 de octubre de 2024.
La mojarra Castarrica (Mayaheros urophthalmus) es propensa a la parasitación debido a su comportamiento alimenticio oportunista. Su distribución abarca cuerpos de agua dulce y salobre en México, especialmente en los estados de Veracruz, Tabasco, Campeche, Chiapas, Yucatán y Quintana Roo, donde es objeto de pesca artesanal para el consumo local. El propósito de esta investigación fue identificar los ectoparásitos presentes en ejemplares silvestres de M. urophthalmus en un ecosistema de manglar en Isla del Carmen, Campeche, México. Se recolectaron un total de 90 ejemplares (longitud media total = 15.1±1.49 cm) para su análisis parasitológico. Se identificaron solo dos especies de parásitos: el copépodo Ergasilus arthrosis en los arcos branquiales y el crustáceo braquiuro Argulus yucatanus en la superficie cutánea de M. urophthalmus. Todos los peces examinados estaban altamente parasitados, con un total de 9,872 individuos de E. arthrosis en los arcos branquiales y 180 individuos de A. yucatanus en los frotis cutáneos. Dada la ubicuidad de los parásitos en las poblaciones de vida silvestre, su presencia no indica necesariamente enfermedad, sino que constituye un indicador de salud ecológica al ser parte integral del equilibrio del ecosistema. Además, dada la falta de conocimiento sobre la parasitofauna específica de la mojarra castarrica en esta región geográfica, este estudio contribuye al conocimiento sistemático de los parásitos de M. urophthalmus en Isla del Carmen, Campeche.
Palabras clave: Copépodos, Ectoparásitos, Manglar, Mayaheros urophthalmus, Parásitofauna.
The mojarra Castarrica (Mayaheros urophthalmus) is susceptible to parasitism due to its opportunistic feeding behavior. Its distribution encompasses freshwater and brackish water bodies in Mexico particularly in the states of Veracruz, Tabasco, Campeche, Chiapas, Yucatán, and Quintana Roo, where it is caught by artisanal fishing for local consumption. The purpose of this research was to identify ectoparasites present in wild specimens of M. urophthalmus in a mangrove ecosystem in Isla del Carmen, Campeche, Mexico. A total of 90 specimens were collected (the average total length (TL) was 15.1 ± 1.49 cm) for parasitological analysis. Only two species of parasites were identified: the parasitic copepod Ergasilus arthrosis found in the in the gill arches and the branchiuran crustacean Argulus yucatanus on the skin surface of M. urophthalmus. All examined fish were heavily parasitized, with a total of 9,872 individuals of E. arthrosis in the gill arches and 180 individuals of A. yucatanus in skin smears. Given the ubiquity of parasites in wildlife populations, does not necessarily indicate disease, but rather constitutes an indicator of ecological health, as they are integral to the ecosystem balance. Furthermore, given the lack of knowledge about the specific parasitofauna of the mojarra Castarrica in this geographic region, this study contributes to the systematic understanding of parasites in M. urophthalmus in Isla del Carmen, Campeche.
Keywords: Copepods, Ectoparasites, Mangrove, Mayaheros urophthalmus, Parasitofauna.
En las últimas décadas se ha reconocido que el parasitismo desempeña un papel fundamental en los ecosistemas. Los parásitos regulan la abundancia y densidad de las poblaciones hospederas, estabilizan la red alimentaria y estructuran las comunidades animales (Lafferty et al., 2008). Además, la extinción de parásitos puede tener consecuencias imprevistas, afectando la salud y abundancia de numerosas especies de vida libre (Dobson et al., 2008). Por lo tanto, un mayor conocimiento sobre la diversidad parasitaria puede contribuir significativamente al manejo y conservación del ambiente (Poulin, 2004a). Los ambientes acuáticos, en particular, han favorecido la diversificación de las especies parásitas, posiblemente debido a la presencia de largas cadenas o redes tróficas (Palm y Klimpel, 2007). Esto se ha demostrado principalmente en peces hospederos, que han recibido considerable atención desde una perspectiva ecológica (Poulin, 2004b). Una razón de esto es que los peces son capturados y examinados con frecuencia en grandes cantidades, lo que aumenta la probabilidad de detectar sus parásitos en comparación con otros vertebrados (Poulin, 2004a). Como resultado, el estudio de las comunidades parásitas en peces ha sobresalido durante las dos últimas décadas (Poulin, 2007a). Entre los peces de agua dulce, el cíclido Mayaheros urophthalmus Günther, 1862 es una especie endémica de la región del Usumacinta, conocida por diversos nombres autóctonos como cíclido maya, mojarra mexicana, mojarra castarrica y cíclido octobarrado. Su distribución geográfica se extiende desde el sur de Veracruz hasta la península de Yucatán y el río Prinzapolka en Nicaragua, a lo largo de la vertiente atlántica de América Central (Espinosa-Pérez et al., 1993). Además, se ha encontrado una población en Isla Mujeres, ya que también toleran el agua salada. Son comunes en las zonas de manglar, pero también se pueden encontrar en cenotes y en ríos de aguas claras y turbias, con sustratos de arena, lodo o rocas. Su abundancia y distribución han dado lugar a una pesquería artesanal en el sureste de México y han sido ampliamente estudiadas para su implementación en cultivos acuícolas (Martínez-Palacios y Ross, 1994). En México, los peces, y en particular los dulceacuícolas, representan el grupo de hospederos más estudiado en busca de helmintos parásitos (Pérez-Ponce de León y García-Prieto, 2001). La Colección Nacional de Helmintos cuenta con una base de datos que incluye alrededor de 4,000 registros de aproximadamente 200 especies de peces dulceacuícolas de México, en los cuales se han registrado cerca de 270 especies de helmintos (Pérez-Ponce de León et al., 1996; Garrido-Olvera et al., 2006; Salgado-Maldonado, 2006). La mojarra castarrica M. urophthalmus es un potencial huésped de parásitos debido a sus hábitos alimenticios oportunistas. En condiciones naturales, la dieta de este pez incluye pequeños crustáceos, insectos, micrófitos y detritos, aunque también se ha adaptado para consumir dietas artificiales desarrolladas a partir de estudios de nutrición (Torchin et al., 2003). Aunque es omnívoro, tiende hacia la carnivoría, convirtiéndose en un depredador tope en su hábitat y controlando las poblaciones de otras especies. La estabilidad de sus poblaciones es crucial para mantener el equilibrio de los ecosistemas acuáticos, especialmente en aquellos donde actúa como depredador tope o forma parte integral de las cadenas tróficas. Este cíclido es un hospedero intermediario o definitivo de numerosos parásitos, incluyendo monogéneos, acantocéfalos, céstodos, nematodos y digéneos (Vidal-Martínez et al., 2000). Por esta razón, se ha utilizado como modelo para estudiar los procesos de colonización y evolución de la helmintofauna asociada. Sin embargo, aunque algunos estudios abarcan todos los grupos de metazoos parásitos encontrados en los peces hospederos (es decir, helmintos y crustáceos), es evidente que se ha puesto mayor énfasis en el estudio de las comunidades de helmintos (Violante-González et al., 2008, 2009; Rodríguez- Santiago et al., 2014). Entre los parásitos externos (ectoparásitos), los copépodos parásitos (Crustacea: Copepoda) representan una parte significativa de la biodiversidad y pueden ser problemáticos para la acuicultura. No obstante, hasta la fecha han recibido poca atención. Los copépodos parásitos son un objeto importante de estudio, ya que solo se ha registrado su presencia en el 1.3% de los invertebrados acuáticos y en el 16% de los peces, lo cual es bajo considerando que cada animal acuático es un hospedero potencial para los copépodos (Ho, 2001). Los branquiuros son parásitos obligados que utilizan como huéspedes a diferentes especies de peces de un amplio rango de familias, encontrándose tanto en peces dulceacuícolas como salobres y marinos. El género Argulus ha cobrado interés en la acuicultura. Actualmente, en México se conocen menos de 10 especies, entre las cuales A. yucatanus infecta a M. urophthalmus. Por lo tanto, dado el escaso conocimiento acerca de la parasitofauna que afecta a la mojarra castarrica en esta región de México, el objetivo del presente estudio fue identificar los ectoparásitos en especímenes silvestres de M. urophthalmus en un ecosistema de manglar en Isla del Carmen, Campeche.
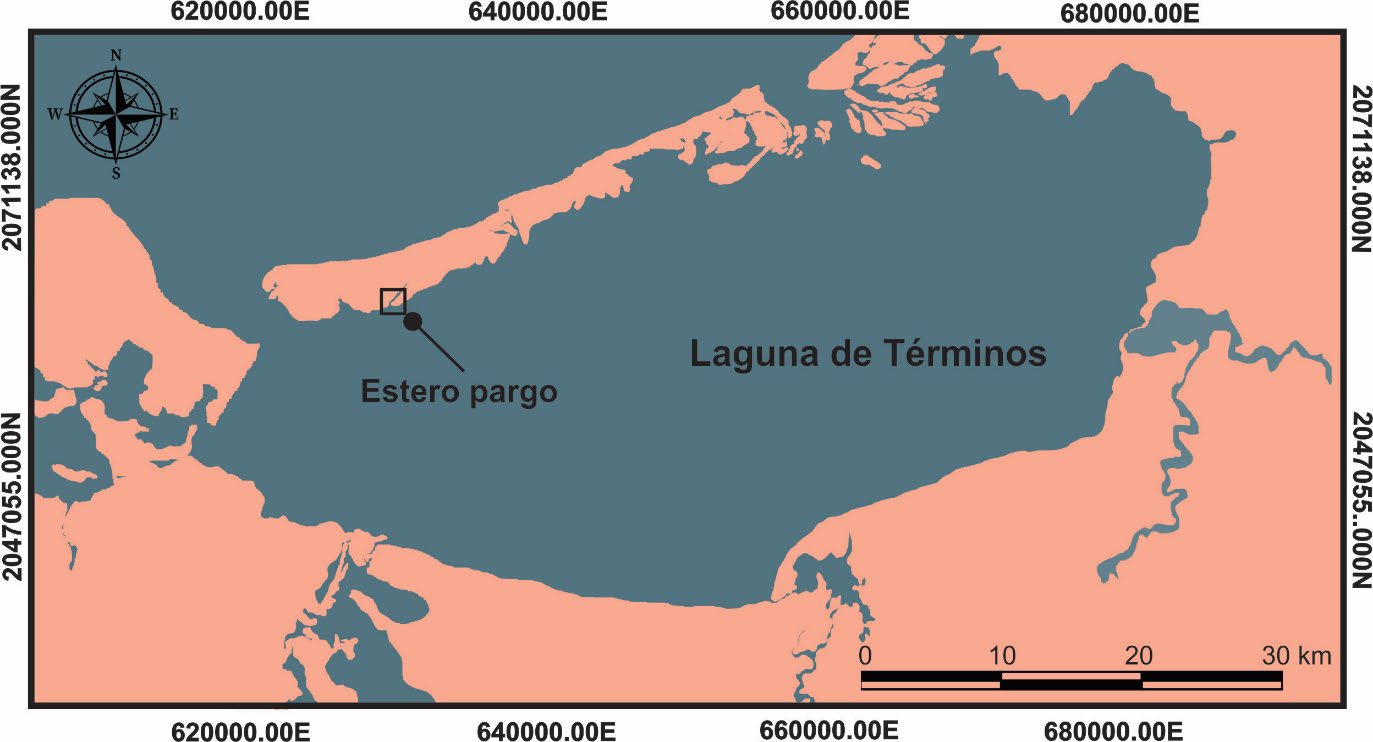
El estudio se realizó en un ecosistema de manglar conocido como “Estero Pargo”, ubicado en Isla del Carmen, Campeche (Fig. 1). Este es un brazo de agua de la Laguna de Términos que se adentra hacia el interior de la isla y está bordeado por manglares.

Localización del sitio de muestreo (Estero Pargo) en Ciudad del Carmen Campeche, México.
En este sistema se capturaron un total de 90 ejemplares de la especie M. urophthalmus, con longitudes de 11.1 a 19.5 cm (promedio ± error estándar = 15.1±1.49 cm) (Fig. 2). Las muestras se obtuvieron entre abril de 2022 y diciembre de 2023, utilizando una red de enmalle de 40 x 2 x 50 mm x 100 m.

M. urophthalmus en el Estero Pargo, Ciudad del Carmen Campeche, México.
Los ejemplares colectados se transportaron individualmente en bolsas de plástico dentro de neveras con hielo, previamente etiquetadas, al Laboratorio Ambiental de Parasitología del Centro de Investigación de Ciencias Ambientales de la Universidad Autónoma del Carmen (Campeche), Ciudad del Carmen, México, para su análisis parasitológico. Los peces fueron sometidos a un examen externo en búsqueda de ectoparásitos, incluyendo la piel, branquias, cavidades nasales y ojos. Los parásitos encontrados se preservaron en viales individuales etiquetados con alcohol etílico al 70% y se procesaron de acuerdo con los métodos descritos por Lamothe-Argumedo (1997), Vidal Martínez et al. (2002) y Guzman-Cornejo et al. (2012). La identificación de especies de parásitos se realizó mediante claves especializadas (Roberts, 1970; Marques, 2014). Las infecciones se evaluaron cuantitativamente utilizando los índices más comúnmente empleados en parasitología: prevalencia (%), abundancia (número de individuos/hospedero) e intensidad (número de individuos/hospedero infectado) media de cada especie de parásito encontrado (Bush et al., 1997). Finalmente, los parásitos fueron depositados en el Laboratorio de Parasitología Ambiental del Centro de Investigación de Ciencias Ambientales de la Universidad Autónoma del Carmen (Campeche). El diagrama metodológico del estudio se muestra en la Figura 3.

Diagrama metodológico del estudio.
Se confirmó que los ectoparásitos encontrados en M. urophthalmus corresponden a las especies de copépodo parásito Ergasilus arthrosis Roberts, 1969, presente en los arcos branquiales, y al braquiuro Argulus yucatanus Poly, 2005, localizado en la superficie de la piel. Ambas especies de parásitos pertenecen al subfilo Crustacea. Todos los peces examinados resultaron parasitados con al menos una de estas especies de ectoparásitos. En los arcos branquiales se encontraron un total de 9,872 individuos de E. arthrosis, mientras que en los frotis realizados en la superficie de la piel se detectaron 180 individuos de A. yucatanus, E. arthrosis tuvo una prevalencia del 100%, una intensidad media de 110 ± 0.90 individuos/hospedero una intensidad media de 109 ± 0.9 individuos/hospedero y una abundancia media de 109 ± 9 individuos/hospedero (Fig. 4). En el caso de A. yucatanus, se observó una prevalencia del 83%, una intensidad media de 2.4 ± 0.13 individuos/hospedero y una abundancia media de 2 ± 0.18 individuos/hospedero (Fig. 4).

(a) Prevalencia (b), abundancia (c) e intensidad media de parásitos de M. urophthalmus.
Aunque la riqueza de especies de parásitos encontrada en esta especie de pez fue relativamente baja, coincide con lo documentado en otros estudios realizados en diferentes estados de México (Vidal-Martínez et al., 2000, 2022). A pesar de que la presencia de crustáceos parásitos representa una amenaza para el desarrollo de la acuicultura, tanto económica como biológicamente, debido a los efectos adversos sobre la salud de los peces y, en consecuencia, sobre su producción (Aneesh et al., 2014), el daño que causan se debe principalmente a su modo de alimentación y adherencia al hospedero. Utilizan estiletes y/o mandíbulas para alimentarse de tejido y sangre, así como ganchos que facilitan la aparición de infecciones secundarias (Lester et al., 2006). En México se conocen aproximadamente seis especies de Argulus, incluyendo A. yucatanus (May-Tec y Mendoza-Franco, 2022). Nuestros resultados concuerdan con los reportados en las costas de Tamaulipas (Golfo de México), donde Rábago-Castro et al. (2011) documentaron una alta prevalencia del copépodo E. cerastes infectando cultivos de Ictalurus punctatus Rafinesque, 1818. De igual manera, se han observado niveles de infección de A. yucatanus en M. urophthalmus en Celestún, Yucatán (May-Tec et al., 2013; Vidal-Martínez et al., 2014). Respecto al género Argulus, se han reportado las siguientes especies: A. chromidis Krøyer, 1863 y A. rhamdiae Wilson, 1936, infectando a Rhamdia guatemalensis Günther, 1864 en Yucatán (Wilson, 1936); A. flavescens Wilson, 1916, infectando a Ariopsis assimilis Günther, 1864 en Chetumal (Suárez-Morales et al., 1998); A. mexicanus Pineda, Paramo y del Rio, 1995, infectando a Atractosteus tropicus Gill, 1863 en Tabasco (Pineda et al., 1995); A. ambystoma Poly, 2003, infectando a Ambystoma dumerilii Dúges, 1870 en Pátzcuaro, Michoacán (Poly, 2003) y A. yucatanus, infectando a M. urophthalmus en Yucatán (Poly, 2005). Recientemente, se ha reportado la presencia del género Argulus en Lagocephalus laevigatus Linnaeus, 1766 (May-Tec et al., 2022; May-Tec & Mendoza-Franco, 2022). Aunque los estudios sobre los crustáceos parásitos aún son limitados, considerando la alta diversidad de potenciales especies de hospederos que habitan los ecosistemas (Rodríguez-Santiago et al., 2016), las especies de parásitos encontradas en M. urophthalmus no representan un riesgo para la salud humana. Desde un punto de vista parasitológico, el consumo de este pez podría ser seguro, a diferencia de lo reportado en otras especies de cíclidos que pueden albergar parásitos patógenos para el ser humano (Acosta-Pérez et al., 2023).
En Mayaheros urophthalmus se identificaron dos especies de ectoparásitos: el copépodo Ergasilus arthrosis y el braquiuro Argulus yucatanus. La especie E. arthrosis fue la especie con mayor prevalencia, intensidad y abundancia media, localizándose exclusivamente en las branquias del hospedero. Ninguna de las especies parásitas registradas en este estudio representa un riesgo patógeno para los seres humanos.
El estudio fue financiado por los proyectos No. 618 ICMyL-UNAM, dirigido por el Dr. E.A.T., y el proyecto No. 1205 del Programa Cátedras CONAHCYT, a cargo de M.A.R.S. Se agradece a José Francisco Eduardo Enrique Velueta Centella por la creación y edición de las imágenes de los ectoparásitos (copépodo parásito y braquiuro), así como de la imagen de la mojarra castarrica. Igualmente, se expresa el agradecimiento a los estudiantes del Laboratorio Ambiental de Parasitología (UNACAR) por su apoyo en el trabajo de campo y de laboratorio. Además, extendemos nuestro reconocimiento a los revisores anónimos, cuyos comentarios y sugerencias contribuyeron significativamente a mejorar este manuscrito. Asimismo, agradecemos al Dr. Alejandro Gómez Ponce por las facilidades brindadas y su apoyo durante el muestreo.
Acosta-Pérez, J., De-la-Rosa-Arana, J., Vega-Sánchez, V., Reyes-Rodríguez, N., Zepeda-Velázquez, A., & Gómez-De-Anda, F. (2023). Tilapia, high socio-economic cichlid fish, as host of trematode parasites with zoonotic potential. Abanico Veterinario, 13, 1-25.
Aneesh, P. T., Sudha, K., Helna, A. K., Anilkumar, G., & Trilles, J. P. (2014). Multiple parasitic crustacean infestation on belonid fish Strongylura velones. ZooKeys, 353, 339-353. https://doi.org/10.3897/zookeys.457.6817
Bush, A. O., Lafferty, K. D., Lotz, J. M., & Shostak, A. W. (1997). Parasitology meets ecology on its own terms: Margolis et al. revisited. The Journal of Parasitology, 83(4), 575-583.
Espinosa, H., Gaspar-Dillanes, M. T., & Fuentes-Mata, P. (1993). Los peces dulceacuícolas mexicanos: Listados faunísticos III. Instituto de Biología, Universidad Nacional Autónoma de México.
Garrido-Olvera, L., García-Prieto, L., & Pérez-Ponce de León, G. (2006). Checklist of the adult nematode parasites of fishes in freshwater localities from Mexico. Zootaxa, 1201, 1-45.
Guzmán-Cornejo, C., García-Prieto, L., Rivas, G., Mendoza-Garfias, B., Osorio- Sarabia, D., & Montiel-Parra, G. (2012). Manual de prácticas de metazoarios parásitos de vertebrados. Universidad Nacional Autónoma de México.
Ho, J. S., Lin, C. L., & Chen, S. N. (2000). Species of Caligus Müller, 1785 (Copepoda: Caligidae) parasitic on marine fishes of Taiwan. Systematic Parasitology, 46, 159–179. https://doi.org/10.1023/A:1006342120411
Lafferty, K. D., Allesina, S., Arim, M., Briggs, C. J., De Leo, G., Dobson, A. P., ... & Thieltges, D. W. (2008). Parasites in food webs: the ultimate missing links. Ecology Letters, 11(6), 533-546.
Lamothe-Argumedo, R. (1997). Manual de técnicas para preparar y estudiar los parásitos de animales silvestres. AGT.
Lester, R. J. G., & Hayward, C. J. (2006). Phylum Arthropoda. En P. T. K. Woo (Ed.), Fish diseases and disorders: Protozoan and metazoan infections (Vol. 1, pp. 466–565). CABI.
Martínez-Palacios, C. A., & Ross, L. G. (1992). The reproductive biology and growth of the Central American cichlid Cichlasoma urophthalmus (Gunther 1862). Journal of Applied Ichthyology, 8, 99-109.
May-Tec, A. L., Pech, D., Aguirre-Macedo, M. L., Lewis, J. W., & Vidal-Martínez, V.M. (2013). Temporal variation of Mexiconema cichlasomae (Nematoda: Daniconematidae) in the Mayan cichlid fish Cichlasoma urophthalmus and its intermediate host Argulus yucatanus from a tropical coastal lagoon.Parasitology, 140, 385-395. https://doi.org/10.1017/S0031182012001734
May-Tec, A. L., Baños-Ojeda, C., & Mendoza-Franco, E. F. (2022). Parasitic crustaceans (Branchiura and Copepoda) parasitizing the gills of puffer fish species (Tetraodontidae) from the coast of Campeche, Gulf of Mexico. ZooKeys, 1089, 73-92. https://doi.org/10.3897/zookeys.1089.79999
May-Tec, A. L., & Mendoza-Franco, E. F. (2022). Variabilidad temporal de crustáceos parásitos de peces y su importancia para el manejo de los recursos costeros ante el cambio climático antropogénico. JAINA Costas y Mares ante el Cambio Climático, 4(1), 63-78. https://doi.org/10.26359/52462.0522
Pérez-Ponce de León, G., García-Prieto, L., Osorio-Sarabia, D., & León-Règagnon, V. (1996). Helmintos parásitos de peces de aguas continentales de México: Listados faunísticos VI. Instituto de Biología, Universidad Nacional Autónoma de México.
Pérez-Ponce de León, G., & García-Prieto, L. (2001). Diversidad de helmintos parásitos de vertebrados silvestres de México. Biodiversitas, 37, 7-11.
Pineda, R., Páramo, S., & Río, R. D. (1995). A new species of the genus Argulus (Crustacea: Branchiura) parasitic on Atractosteus tropicus (Pisces: Lepisosteidae) from Tabasco, Mexico. Systematic Parasitology, 30, 199–206. https://doi.org/10.1007/BF00010470
Poly, W. J. (2003). Argulus ambystoma, a new species parasitic on the Salamander Ambystoma dumerilii from Mexico (Crustacea: Branchiura: Argulidae). Ohio Journal of Science, 103, 52–61.
Poly, W. J. (2005). Argulus yucatanus sp. nov. (Crustacea: Branchiura) parasitic on Cichlasoma urophthalmus from Yucatan, Mexico. Gulf and Caribbean Research, 17, 1-13. https://doi.org/10.18785/gcr.1701.01
Poulin, R. (2004). Macroecological patterns of species richness in parasite assemblages. Basic and Applied Ecology, 5(5), 423-434.
Poulin, R. (2007). Are there general laws in parasite ecology? Parasitology, 134(6), 763-776.
Rábago-Castro, J., Sánchez-Martínez, J. G., Loredo-Osti, J., Gomez-Flores, R., Tamez-Guerra, P., & Ramírez-Pfeiffer, C. (2011). Temporal and spatial variations of ectoparasites on cage-reared channel catfish (Ictalurus punctatus) in Tamaulipas, Mexico. Journal of the World Aquaculture Society, 42(3), 406-411. https://doi.org/10.1111/j.1749-7345.2011.00480.x
Rodríguez-Santiago, M. A., Gómez, S., Rosales-Casián, J. A., & Grano-Maldonado, M. I. (2015). Parasitic copepods of the vermilion rockfish Sebastes miniatus (Pisces: Scorpaenidae) from inshore waters of Baja California (Eastern Pacific). Neotropical Helminthology, 9, 1–12.
Rodríguez-Santiago, M. A., Morales-Serna, F. N., Gómez, S., & Grano-Maldonado, M. I. (2016). New records of parasitic copepods (Copepoda: Pandaridae, Eudactylinidae, Caligidae) on elasmobranchs (Chondrichthyes) in the Gulf of Mexico. Ciencia Pesquera, 24, 15-21.
Salgado-Maldonado, G., & Rubio-Godoy, M. (2014). Parásitos de peces de agua dulce introducidos. En R. Mendoza & P. Koleff (Coords.), Especies acuáticas invasoras en México (pp. 269-285). Comisión Nacional para el Conocimiento y Uso de la Biodiversidad. Suárez-Morales, E., & Reid, J. W. (1998). An updated list of the free-living freshwater copepods (Crustacea) of Mexico. The Southwestern Naturalist, 43, 256-26 Torchin, M. E., Lafferty, K. D., Dobson, A. P., McKenzie, V. J., & Kuris, A. M. (2003). Introduced species and their missing parasites. Nature, 421, 628-630.
Vidal-Martínez, V. M., Centeno-Chalé, O. A., Torres-Irineo, E., Sánchez-Ávila, J., Gold-Bouchot, G., & Aguirre-Macedo, M. (2014). The metazoan parasite communities of the shoal flounder (Syacium gunteri) as bioindicators of chemical contamination in the southern Gulf of Mexico. Parasites & Vectors, 7(1), 1-14.
Vidal-Martínez, V. M., Kennedy, C. R., & Clive, R. (2000). Interacciones potenciales entre los helmintos intestinales del pez cíclido Cichlasoma synspilum del sureste de México. Journal of Parasitology, 86(4), 691-695.
Vidal-Martínez, V. M., Aguirre-Macedo, M. L., Scholz, T., González-Solís, D., & Mendoza-Franco, E. F. (2002). Atlas de los helmintos parásitos de cíclidos de México. Instituto Politécnico Nacional.
Violante-González, J., Aguirre-Macedo, M. L., & Vidal-Martínez, V. M. (2008). Temporal variation in the helminth parasite communities of the Pacific fat sleeper (Dormitator latifrons) from Tres Palos Lagoon, Guerrero, Mexico. Journal of Parasitology, 94, 326-334.
Violante-González, J., Monks, S., Gallegos-Navarro, Y., Santos-Bustos, N. G., Villalba-Vásquez, P. J., Padilla-Serrato, J. G., & Pulido-Flores, G. (2020). Interannual variation in the metazoan parasite communities of bigeye trevally (Caranx sexfasciatus). Parasite, 27, 6. https://doi.org/10.1051/parasite/2020001